Sinovial HL Inj Sol 3.2 % Fertspr 2 ml
Sinovial HL Inj Lös 3.2 % Fertspr 2 ml
-
382.00 CHF

- Availability: Out of stock
- Brand: INS. BIOCHIMIQUE SA
- Product Code: 7531640
- M09AX01
- Size 7612291146768
Active ingredient: Natriumchlorid, Natrium phosphate, Hyaluronsäure, Natriumsalz 64 mg.

Description
Medizinprodukt
Zusammensetzung
1 vorgefüllte 2,25 ml-Einwegspritze aus Glas enthält: 32 mg (H-HA) + 32 mg (L-HA) Hyaluronsäure-Natriumsalz in 2 ml mit Natriumchlorid gepufferter physiologischer Lösung.
Der Inhalt der Spritzen ist steril und pyrogenfrei.
Indikationen/Anwendungsmöglichkeiten
Schmerzen oder eingeschränkte Beweglichkeit infolge degenerativer (Arthrose) oder posttraumatischer Veränderungen der Gelenke oder damit einhergehender Tendinopathien.
Sinovial HL eignet sich als Gelenkflüssigkeitsersatz für die Wiederherstellung der physiologischen und rheologischen Bedingungen arthrotischer Gelenke.
Dosierung/Anwendung
Die Behandlung kann bis zu drei Injektionen betragen, je nach Schweregrad der Gelenksdegeneration. Die Zweckmässigkeit und die Häufigkeit, mit der die Behandlung wiederholt werden kann, müssen vom behandelnden Arzt für jeden Patienten individuell bewertet werden, wobei das Nutzen-Risikoverhältnis der Behandlung jedesmal abgewogen werden sollte.
Ein allenfalls vorhandener Gelenkerguss ist vor der Injektion von Sinovial HL abzusaugen.
| Die Spritzenkappe sorgfältig abschrauben, den Verschlussring der Luer-Lock-Halterung fest zwischen den Fingern halten und gut darauf achten, die Öffnung der Einwegspritze nicht zu berühren (Fig. A). |
| Die in der Packung enthaltene Nadel (Kanülengrösse 21 G) fest in den Luer-Gewindeanschluss der Einwegspritze schrauben bis ein leichter Gegendruck spürbar ist, um eine dichte Verbindung sicherzustellen und damit ein Austreten der Flüssigkeit während der Verabreichung zu verhindern, den Verschlussring des Luer-Lock fest zwischen den Fingern haltend (Fig. B). |
Sinovial HL bei Raumtemperatur und unter strikter Wahrung von Asepsis injizieren. Sinovial HL ist nur in den Gelenkspalt zu injizieren.
Die intraartikuläre Injektion darf nur von einem Arzt vorgenommen werden.
Kontraindikationen
Sinovial HL darf nicht in ein infiziertes oder stark entzündetes Gelenk injiziert oder bei Patienten mit einer Hauterkrankung oder einer Infektion im Bereich der Injektionsstelle angewendet werden.
Warnhinweise und Vorsichtsmassnahmen
Die Injektionsstelle muss in einem Bereich gesunder Haut liegen.
Nicht intravaskulär injizieren, nicht ausserhalb des Gelenkspaltes injizieren, nicht ins Synovialgewebe oder in die Gelenkkapsel injizieren.
Bei einem schwerwiegenden intraartikulären Erguss sollte Sinovial HL nicht angewandt werden.
Nach der intraartikulären Injektion sollte dem Patienten empfohlen werden, jegliche körperliche Anstrengung zu unterlassen und seine normalen Aktivitäten erst nach einigen Tagen wieder aufzunehmen.
Sinovial HL sollte nicht mit Desinfektionsmitteln wie quartäre Ammoniumverbindungen oder Chlorhexidin vermischt werden, da die Hyaluronsäure in der Lösung präzipitieren könnte.
Interaktionen
Bis heute sind keine Interaktionen von Sinovial HL mit anderen Arzneimitteln bekannt.
Basierend auf den zur Zeit verfügbaren in-vitro Daten, sind keine chemisch-physikalischen und biologischen Interaktionen bekannt zwischen Sinovial HL und PRP (Plasma Reich an Blutplättchen), das für die intraartikuläre Infiltrationstherapie von Osteoarthrose verwendet wird.
Unerwünschte Wirkungen
Sinovial HL kann lokal zu unerwünschten Wirkungen führen.
Bei der Anwendung von Sinovial HL können an der Einstichstelle Begleiterscheinungen wie Schmerzen, Hitzegefühl, Rötungen oder Schwellungen auftreten. Solche Begleiterscheinungen lassen sich durch Auflegen eines Eisbeutels auf das behandelte Gelenk mildern. Sie klingen in der Regel nach kurzer Zeit wieder ab.
Der Arzt sollte sicherstellen, dass ihn seine Patienten über allfällig später auftretende unerwünschte Wirkungen informieren.
Eigenschaften/Wirkungen
Hyaluronsäure-Natriumsalz besteht aus sich wiederholenden Ketten von Disaccharid-Einheiten aus N-Acetylglucosamin und Natriumglucuronat. Es ist ein wesentlicher Bestandteil der Synovialflüssigkeit und verleiht dieser ihre viskoelastischen Eigenschaften.
Sinovial HL besteht aus einer physiologischen Lösung, gepuffert mit Hyaluronsäure von hohem Molekulargewicht (H-HA) und niedrigem Molekulargewicht (L-HA).
Die in Sinovial HL enthaltene, fermentativ gewonnene und chemisch nicht modifizierte Hyaluronsäure mit hohem und niedrigem Molekulargewicht wird sehr gut vertragen. Zudem, dank einer spezifischen und patentierten Behandlung der Lösung, interagieren die in Sinovial HL enthaltenen HA-Ketten unterschiedlicher Molekulargewichte miteinander und verleihen Sinovial HL einzigartige rheologische Eigenschaften, die bei gleicher Lösungsviskosität die Verabreichung von höheren Konzentrationen an Hyaluronsäure ermöglichen. Indem Sinovial HL die viskoelastischen Eigenschaften der Gelenkflüssigkeit wieder herstellt, reduziert es den Schmerz und verbessert es die Beweglichkeit der Gelenke und der Sehnen.
Sinovial HL wirkt nur in den Gelenken, in die es injiziert wird. Es entfaltet keinerlei systemische Wirkung.
Weitere Bestandteile von Sinovial HL sind Natriumchlorid, Natriumphosphat und Wasser für Injektionszwecke.
Sonstige Hinweise
Darf nur gegen ärztliches Rezept abgegeben werden.
Ampullenspritze dampfsterilisiert.
Nadel mit Ethylenoxid sterilisiert.
Der Inhalt der vorgefüllten Spritze ist steril. Die Spritze und die Nadel sind in einem versiegelten Blister verpackt.
Die äussere Spritzenoberfläche ist nicht steril.
Sinovial HL darf nur bis zu dem auf der Packung angegebenen Verfalldatum verwendet werden.
Wenn die Packung bereits offen oder beschädigt ist, sollte Sinovial HL nicht mehr angewendet werden.
Nicht erneut sterilisieren. Der Inhalt einer Spritze ist nur zur einmaligen Anwendung bestimmt.
Nicht wieder verwenden, um jegliche Kontaminationsgefahr zu vermeiden.
Bei Raumtemperatur, aber auf jeden Fall unter 25 °C, sowie von Wärmequellen entfernt aufbewahren. Nicht einfrieren.
Nach dem Öffnen muss Sinovial HL sofort verwendet und nach Gebrauch entsorgt werden.
Ausserhalb der Reichweite und Sicht von Kindern aufbewahren.
Das eventuelle Vorhandensein einer Luftblase beeinträchtigt keineswegs die Produkteeigenschaften.
Vertriebsfirma
IBSA institut Biochimique SA, CH 6903 Lugano.
Herstellerin
IBSA Farmaceutici Italia Srl, Via Martiri di Cefalonia, 2 - 26900 Lodi – Italien.
Stand der Information
Juli 2018.
Dispositif médical
Composition
1 seringue en verre pré-remplie à usage unique de 2,25 ml contient: 32 mg (H-HA) + 32 mg (L-HA) d'acide hyaluronique sel sodique dans 2 ml de solution physiologique tamponnée de chlorure de sodium.
Le contenu de la seringue est stérile et apyrogène.
Indications/Possibilités d’emploi
Douleurs ou limitations de la mobilité en cas d’altérations dégénératives (arthrose) ou post-traumatiques des articulations ou en cas de tendinopathies associées.
Sinovial HL est un agent de substitution au liquide articulaire approprié qui permet de rétablir les conditions physiologiques et rhéologiques des articulations arthrosiques.
Posologie/Mode d’emploi
Le traitement peut aller jusqu’à trois injections selon la gravité de la dégénérescence articulaire. L’opportunité et la fréquence avec laquelle le traitement peut être répété doivent être évaluées par le médecin pour chaque patient individuellement, prenant en considération pour chaque cas le rapport risque/bénéfice du traitement.
Aspirer un éventuel épanchement articulaire avant d'injecter Sinovial HL.
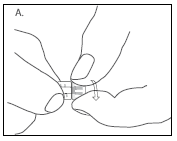 | Dévisser soigneusement le capuchon de la seringue, tout en tenant fermement le collet du raccord Luer-Lock et faisant particulièrement attention à ne pas toucher son orifice (Fig. A). |
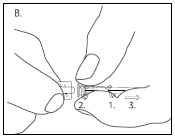 | Insérer l’aiguille de diamètre 21 G incluse dans la confection, la vissant dans le raccord Luer-Lock jusqu’à percevoir une légère résistance, pour assurer un raccordement étanche et prévenir toute fuite de liquide lors de l’administration (Fig. B). |
Injecter Sinovial HL à température ambiante et sous stricte observation des règles d’asepsie. Injecter Sinovial HL uniquement à l’intérieur de l’espace synovial.
L’injection intra-articulaire ne peut être effectuée que par un médecin.
Contre-indications
Sinovial HL ne doit pas être injecté en présence d’une articulation infectée ou fortement enflammée ou si le patient présente une affection cutanée ou une infection au niveau du site de l'injection.
Mises en garde et précautions
Le point d'injection doit être situé sur peau saine.
Ne pas injecter par voie intra-vasculaire. Ne pas injecter en dehors de l'interligne articulaire, dans le tissu synovial ou dans la capsule articulaire.
Ne pas administrer Sinovial HL en présence d'un épanchement intra-articulaire important.
Après l’injection intra-articulaire, il faudra recommander au patient de s'abstenir de tout effort physique et de ne reprendre ses activités normales qu'après quelques jours seulement.
Ne pas mélanger Sinovial HL avec des désinfectants du type sels d’ammonium quaternaires ou chlorhexidine à cause du risque de précipitation de l’acide hyaluronique dans la solution.
Interactions
Aucune interaction de Sinovial HL avec d’autres médicaments n’a été rapportée à ce jour.
Sur la base des données in vitro disponibles aujourd’hui, aucune interaction chimique, physique ou biologique entre le Sinovial HL et le PRP (plasma riche en plaquettes), employé pour le traitement infiltrant endo-articulaire de l’arthrose, n’a été rapportée.
Effets indésirables
L’infiltration extra-articulaire de Sinovial HL peut causer des effets secondaires locaux.
Durant l’emploi de Sinovial HL, des symptômes comme des douleurs, sensations de chaleur, rougeurs ou gonflements peuvent survenir au niveau du site d'injection. L'application de glace sur l'articulation traitée permet de soulager de tels effets secondaires. Généralement ceux-ci régressent en peu de temps.
Le médecin doit s’assurer que les patients l’informent d’éventuels effets indésirables survenus après le traitement.
Propriétés/Effets
L’acide hyaluronique sel sodique se compose de chaînes itératives d’unités disacharidiques de N-acétylglucosamine et glucuronate de sodium. Il constitue un composant essentiel du liquide synovial auquel il confère ses propriétés viscoélastiques.
Sinovial HL est une solution physiologique tamponnée d'acide hyaluronique à haut poids moléculaire (H-HA) et à bas poids moléculaire (L-HA).
L’acide hyaluronique à haut et bas poids moléculaire utilisé dans le dispositif est obtenu par fermentation et n’est pas modifié chimiquement, ce qui lui confère une excellente tolérance. En outre, grâce à un traitement spécifique et breveté de la solution, les chaînes HA de divers poids moléculaires interagissent entre elles, conférant à Sinovial HL des propriétés rhéologiques uniques qui permettent d’administrer des concentrations plus élevées d’acide hyaluronique. En rétablissant les propriétés viscoélastiques du liquide articulaire, Sinovial HL réduit la douleur et rétablit la mobilité articulaire et des tendons.
Sinovial HL n’agit qu’au niveau de l’articulation dans laquelle il a été injecté et n'exerce aucun effet systémique.
Les autres composants du produit sont du chlorure de sodium, du phosphate de sodium et de l'eau pour préparations injectables.
Remarques particulières
Ne peut être délivré que sur prescription médicale.
Ampoule-seringue stérilisée par chaleur humide.
Aiguille stérilisée à l’oxyde d’éthylène.
Le contenu de la seringue pré-remplie est stérile. La seringue et l’aiguille sont confectionnées dans un blister hermétique.
La surface extérieure de la seringue n’est pas stérile.
Ne pas utiliser Sinovial HL au-delà de la date limite figurant sur l'emballage.
Ne pas employer Sinovial HL si l’emballage résulte déjà ouvert ou endommagé.
Ne pas re-stériliser. Le contenu de la seringue est à usage unique exclusivement.
Ne pas réutiliser afin d’éviter tout risque de contamination.
Conserver à température ambiante en tout cas inférieure à 25 °C et à l’écart de sources de chaleur. Ne pas congeler.
Une fois ouvert, Sinovial HL doit être utilisé immédiatement et être éliminé après l’emploi.
Tenir hors de la portée et de la vue des enfants.
L’éventuelle présence d’une bulle d’air ne compromet pas les caractéristiques du produit.
Distribution
IBSA Institut Biochimique SA, 6903 Lugano.
Fabricant
IBSA Farmaceutici Italia Srl, Via Martiri di Cefalonia 2, 26900 Lodi – Italie.
Mise à jour de l’information
Juillet 2018.




 Deutsch
Deutsch Französisch
Französisch




